Что такое метиловый спирт, Метиловый спирт
Простое включение системы позволяло двигателю поглотить больше воздуха, благодаря охлаждающему эффекту, тем самым увеличивая производительность примерно на л. Симптомы и формы интоксикации. Потолки 3,6 м. Высокая температура кипения метанола и хорошая его растворимость в воде объясняется полярностью связи в гидроксильной группе — ОН. Поговорим еще раз об отравлении метиловым спиртом.
Были разработаны процессы парофазной высокотемпературной газификации угля и кокса , в результате которой получали газы, содержащие оксид углерода и водород. Эти газы нашли применение для уличного освещения городов под названием « светильный газ ». Используя водород , произведённый по той же технологии, Фриц Габер и Карл Бош разработали промышленный метод гидрирования молекулярного азота до аммиака при очень высоких температурах и давлениях.
Это позволило разработать другие промышленные химические процессы переработки аналогичного сырья в условиях высоких температур и давлений, например, синтез метанола. Так как синтез метанола аналогичен с синтезом аммиака , то, их часто производят на одном и том же заводе.

Синтез метанола путем взаимодействия монооксида углерода с водородом впервые предложил в году французский химик Поль Сабатье [3]. После Первой мировой войны « BASF » возобновила свои исследования по синтезу метанола и в году построила в Лойне Германия первую промышленную установку по синтезу метанола при высоком давлении.
В период между годом и годом Ф. Фишер [5] и Г. Тропш , химики лаборатории по исследованию угля в Германии в городе Мюльхайме , опубликовали подробные результаты изучения возможности синтеза углеводородов , в том числе синтеза метанола из синтез-газа смеси угарного газа и водорода.
Эти работы легли в основу технологического процесса, известного как синтез Фишера — Тропша [3]. В году в США корпорация « Commercial Solvent Corporation » использовала технологию синтеза под высоким давлением для превращения в метанол смесей диоксида углерода с водородом , образующихся как побочные газообразные продукты ферментации.
В то же время компания «DuPont» на том же самом заводе приступила к производству метанола и аммиака из синтез-газа, полученного из угля. В е годы в США был внедрен технологический процесс парофазной конверсии природного газа , в основу которого легли исследования, проведенные в BASF в е годы. С тех пор уголь стал все меньше и меньше использоваться как сырьё для получения синтез-газа , и ему на смену пришёл более чистый и дешёвый природный газ , запасы которого в недрах оказались огромными [3].
В е годы для синтеза метанола стали использовать в качестве сырья сырую нефть и керосин в небольших количествах. В паровой конверсии метана получался синтез — газ высокого качества. Это позволило внедрить технологии синтеза метанола при низком давлении. В настоящее время процесс синтеза метанола при низком давлении широко используется в органическом синтезе.
Применение активных катализаторов стало возможным благодаря использованию в качестве сырья синтез-газа с пониженным содержанием каталитических ядов сера , её органические и неорганические соединения , и карбонилы металлов. За последние 40 лет процесс синтеза метанола из оксидов углерода в СО присутствует некоторое количество диоксида углерода и водорода был усовершенствован и доработан.
Сегодня в мире почти весь метанол получают из синтез-газа. В настоящее время исследовательские работы направлены на развитие новых способов синтеза метанола при ещё более низких температурах и давлении. Изучается возможность использования в качестве сырья смеси оксидов углерода и водорода из разнообразных источников, а также возможность синтеза метанола прямым окислением метана , минуя стадию образования синтез-газа , а также через гидрирование диоксида углерода , полученного химической утилизацией углекислого газа.
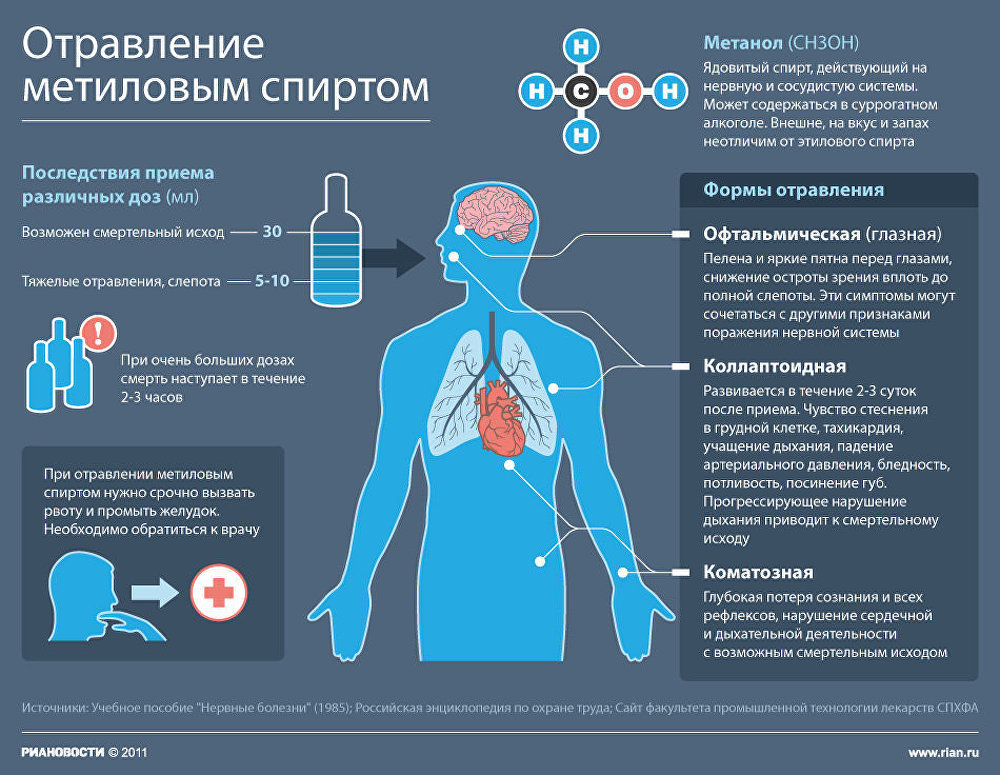
С точки зрения экономии энергоресурсов такой метод получения метанола является наилучшим. Метанол — очень токсичное органическое вещество, яд , действующий на нервную и сосудистую системы.
При обычных условиях это бесцветная, легколетучая, горючая жидкость , иногда с запахом, напоминающим запах этилового спирта. На организм человека метанол действует опьяняющим образом и является сильным ядом , вызывающим потерю зрения при приёме во внутрь мл метилового спирта возможно тяжёлое отравление и, в зависимости от дозы , смерть при попадании 30 мл и более. Теплопроводные свойства метанола в два раза меньше, чем у бензина.
Метанол участвует в образовании взрывоопасных веществ из-за собственной горючести. Метиловый спирт смешивается во всех соотношениях с водой и большинством органических растворителей , обладает всеми свойствами одноатомных спиртов [8]. Физические характеристики метанола приведены в таблице 1 [9].
Гидроксильная группа — ОН в структуре молекулы метанола является функциональной группой и определяет его физические и химические свойства. Высокая температура кипения метанола и хорошая его растворимость в воде объясняется полярностью связи в гидроксильной группе — ОН.
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода. В образовании химических связей с атомами углерода и водорода участвуют две 2sp 3 — гибридные орбитали , еще две 2sp 3 — гибридные орбитали заняты неподеленными электронными парами атома кислорода. Поэтому валентный угол C — О — H близок к тетраэдрическому и составляет почти о [1]. Между молекулами спирта имеют место межмолекулярные водородные связи , которые способствуют притяжению и ассоциации молекул спиртов.
Межмолекулярные водородные связи и объясняют высокую температуру кипения метанола и жидкое агрегатное состояние при обычных условиях. Водородные связи образуются в водных растворах между молекулой метанола и воды, то есть молекулы метанола в воде гидратируются. Этим объясняется хорошая растворимость метанола в воде [1].
Метанол обладает свойствами очень слабого основания и слабой кислоты. Метанол — неэлектролит , в водном растворе на ионы не диссоциирует , поэтому кислотные свойства более слабые по сравнению с водой [12]. Как метанол , так и этанол также легко воспламеняются в любом агрегатном состоянии.
При этом их реакции горения могут быть полными или неполными. Кроме того, они не подвергаются ионной диссоциации, в результате чего имеют нейтральный pH. Несмотря на то, что человечество пользуется свойствами спиртов уже тысячи лет, метанол был открыт только в г. Его автором был британский химик и физик Роберт Бойль, который провел перегонку древесины самшит — отсюда и альтернативное название соединения: древесный спирт.
Только в году французским исследователям удалось определить структуру молекулы. Именно тогда был введен термин «метиловый спирт». С точки зрения человека, два наиболее важных свойства метанола — это его сильная токсичность и тот факт, что он является отличным растворителем. Первое свойство означает опасность его использования, а благодаря второму он нашел широкое применение. Поскольку метанол является ядом, его ни в коем случае нельзя употреблять или вдыхать.
Даже доза в 10 мл метаболизируется в муравьиную кислоту. Она может разрушить зрительный нерв, вызывая постоянную слепоту. Дальнейшие негативные последствия воздействия включают гипоксию на клеточном уровне, метаболический ацидоз и другие нарушения, приводящие даже к смерти. Смертельной дозой считается 15 мл чистого метанола.
Однако для химической промышленности метиловый спирт является прежде всего важным компонентом ключевых реакций. Благодаря легкому превращению в формальдегид, углеводороды и метиламин, он используется для производства широкого спектра товаров повседневного спроса. Ежегодно в мире производится до 20 миллионов тонн метанола. Однако основным методом получения токсичного соединения является уже не перегонка древесины, а реакция гидрогенизации угарного газа в присутствии катализатора.
Чаще всего этот процесс сопровождает производство биомассы. Метанол используется в фармацевтической промышленности, в производстве пластмасс и синтетических тканей, а также красителей, фунгицидов и даже фотопленок. Пока он правильно маркирован и ответственно используется, он выполняет важную экономическую функцию.
К сожалению, до сих пор есть немало случаев серьезного отравления метанолом. С химической точки зрения этанол является ближайшим родственником метанола. В одной молекуле он содержит на один атом углерода и два атома водорода больше. Это, на первый взгляд, небольшое отличие, однако, частично меняет свойства этилового спирта, делая его более безопасным для человека. К сведению, стоит отметить, что безопасность слишком часто бывает иллюзорной!
Также как метанол, он является эффективным растворителем и участвует во многих важных реакциях синтеза. Интересно, что он естественным образом вырабатывается дрожжами, метаболизирующими сахар.
Этот механизм используется при ферментации пива или вина. Летальность при отравлении метиловым спиртом значительна.
Хронические отравления характеризуются головокружением, головной болью, бессонницей, повышенной утомляемостью, желудочно-кишечными расстройствами, болями в области сердца и печени, нарушением функции зрения, прежде всего цветного. Приложение: Памятка. Администрация Дума Контрольно-счетный орган.
Опубликовано